REVISIÓN BIBLIOGRÁFICA
Fibrilación Auricular: de Arritmia Infradiagnosticada a Epidemia Cardiológica
Atrial Fibrillation: From Infradiagnosed Arrhythmia to Cardiological Epidemic
Dr. José Apolo 1; Dra. Ailema Alemán 2
1. 2. Unidad de Cardiología y Electrofisiología del HCSA
Palabras Clave: Fibrilación auricular, arritmia cardiaca
Keywords: Atrial fibrillation, cardiac arrythmia
Fecha recepción: 10-01-2022
Fecha aceptación: 17-03-2022
Fecha publicación: 20-04-2022
DOI: 10.65183/revind.e4.05
Resumen
La fibrilación auricular es la arritmia cardiaca sostenida más frecuente en la población general. Se estima que las personas mayores de 40 años presentan una prevalencia del 5% de esta arritmia. La incidencia y dimensión de la fibrilación auricular se mantiene en constante aumento y la Organización Mundial de la Salud (OMS) la cataloga como una nueva epidemia; las posibles causas de esta situación son la mayor esperanza de vida, las nuevas herramientas diagnósticas y el incremento de los factores de riesgo tanto en sociedades de primer mundo como en países en vías de desarrollo. El presente trabajo presenta una revisión de la epidemiología, fisiopatología, complicaciones y manejo actual de la fibrilación auricular.
Abstract
Atrial fibrillation is the most common sustained cardiac arrhythmia in the general population. It is estimated that people over 40 years of age have a 5% prevalence of this arrhythmia. The incidence and prevalence of atrial fibrillation is constantly increasing and the World Health Organization (WHO) classifies it as an epidemic; the possible causes of this are the longer life expectancy, the new diagnostic tools and the increase in risk factors both in first world societies and in developing countries. The present work presents a review of the epidemiology, pathophysiology, complications and current management of atrial fibrillation.
Introducción
Debido a que la alta incidencia de la fibrilación auricular (FA) constituye una importante carga para pacientes, personal sanitario y sistemas de salud, las consecuencias de la FA se han establecido claramente en múltiples estudios de cohortes observacionales, e incluyen un aumento de las tasas de accidente cerebrovascular (ACV), demencia, insuficiencia cardiaca y embolia sistémica en ausencia de una correcta anticoagulación oral, con un crecimiento de la morbilidad y la mortalidad 1-4. El coste de esta entidad por los servicios de salud cada vez es más alto, estimándose en 1% del presupuesto de Servicio Nacional del Salud en el Reino Unido y entre 16 a 26 billones de dólares en gastos anuales por atención de manera directa o derivado de sus complicaciones en los Estados Unidos 5-7.
Este artículo presenta un resumen de la evidencia disponible sobre fibrilación auricular; de este modo, se intenta demostrar de manera comprensible a todo el personal de salud la información más relevante a tener en cuenta al momento de enfrentar esta patología y la importancia de su adecuado tratamiento temprano.
Definición
La fibrilación auricular se trata de una taquicardia supraventricular caracterizada por actividad eléctrica caótica (desorganizada y rápida) y la pérdida de la actividad mecánica auricular con ausencia de contracción efectiva; de esta manera, la expulsión de sangre se realiza de manera inadecuada, permaneciendo retenida en la cavidad auricular y orejuela 8-9.
Asimismo, esta afección muestra algunas características electrocardiográficas diagnósticas, como son ausencia de onda P antes del QRS, intervalos R-R irregulares y frecuencia auricular >300 lpm.
PRESENTACIÓN MUNDIAL DE LA FA
Debido a sus particularidades clínicas y formas de manifestarse, estimar la carga real de FA en la población general representa un reto científico, y, según la Organización Mundial de la Salud (OMS), el mundo afronta una epidemia por FA, ya que se estima que del 1 al 5% de la población mundial menor de 60 años y casi el 20% de los mayores de 80 años la presentan. Por otro lado, las estadísticas revelan una gran masa poblacional no diagnosticada, estimándose en este caso un 1%de la población mayor de 40 años y un 1-5% de mayores de 65 años; de entre estos pacientes, aproximadamente el 70% tiene riesgo elevado de ACV2. Chugh, et al. 4 realizaron una revisión sistemática de más de 180 estudios poblacionales de valoración estadística de la FA, de 1980 al 2010, demostrando mayor incidencia de esta en países desarrollados, en sexo masculino y predominio de presentación en pacientes mayores de 65 años (figura 1).
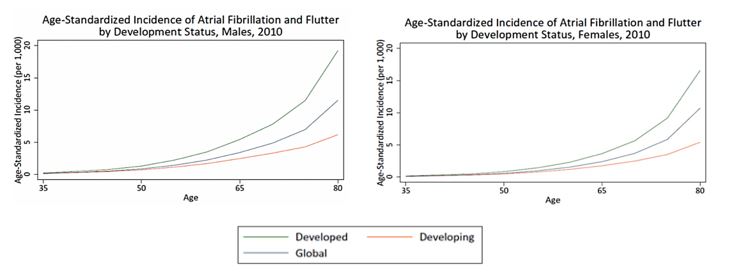
Figura 1.- FA presenta un aumento en su incidencia después de los 65 años y de forma predominante en países desarrollados.
Complicaciones
La fibrilación auricular aumenta el riesgo de acciden- te cerebrovascular tromboembólico cinco veces, como resultado de la acumulación de sangre en la aurícula izquierda y embolización sistémica al cerebro. Los pa- cientes con ACV tromboembólico presentan mayor mor- talidad, mayor morbilidad y estancias hospitalarias más prolongadas que los pacientes con otros subtipos de ac- cidente cerebrovascular 7; además, en los pacientes con FA, existe un riesgo aumentado de otras complicaciones: se incrementa al doble el riesgo de demencia, se triplica el riesgo de sufrir insuficiencia cardíaca y, por lo tanto, de ingresos hospitalarios, y aumenta en un 40% el riesgo de mortalidad total 10, sin contar la calidad de vida y el número elevado de fármacos que deben recibir.
Fisiopatología
De modo general, las arritmias necesitan para su desarrollo la confluencia de tres factores esenciales: uno es el mecanismo disparador, otro el perpetuador, ambos bajo la influencia del sistema nervioso autónomo, que constituiría el tercer elemento.
La fibrilación auricular debuta en forma de episodios paroxísticos y evoluciona hacia la persistencia, sin embargo, esta transformación se produce de modo muy diverso y no resulta posible predecir cuándo ocurrirá, algunos pacientes podrán permanecer con episodios paroxísticos durante largos períodos de tiempo, mientras que otros pasarán a la forma persistente con mucha mayor antelación 11. Se estima que, en aquellos pacientes en los que predominen los cuadros paroxísticos, existirá mayor relación con los mecanismos de trigger o disparadores y que, en aquellos con avance rápido a formas persistentes, predominarán los factores perpetuadores. Dentro de los mecanismos fisiopatológicos, se encuentran la degeneración del tejido auricular con incremento de la fibrosis, deterioro del sistema normal de conducción, progresión de las enfermedades cardiacas estructurales, la presencia de cardiopatía isquémica, valvulopatías, las enfermedades inflamatorias e infiltrativas, los desequilibrios hidroelectrolíticos y metabólicos, algunos medicamentos y el sistema nervioso autónomo.
Numerosos estudios han demostrado como principal mecanismo disparador de FA las extrasístoles a nivel de las venas pulmonares (cerca del 94% de los casos) 12 y, con menor frecuencia, la vena cava superior, el ligamento de Marshall y el seno coronario entre otros. Nos centraremos en los mecanismos más estudiados.
Rol de las venas pulmonares. — Para entender el papel de las venas pulmonares como mecanismo disparador, destacaremos que existen dos características anatómicas esenciales en la arquitectura de estas, que guardan relación con su papel en la génesis de la arritmia. Una de ellas es la presencia de brechas de tejido fibroso entre los haces musculares y la segunda las conexiones mio- cárdicas de las mismas al subepicardio y subendocardio auricular 13. Además, la disposición espacial de las fibras con distribución circunferencial y longitudinal favorece la conducción anisotrópica de los potenciales eléctricos favoreciendo el mecanismo arrítmico de microreentrada, substrato esencial para el inicio de la fibrilación auricular 14.
Los pacientes con fibrilación auricular presentan características electrofisiológicas diferentes a los pacientes sanos. Sus periodos refractarios atriales son más cortos, lo que conlleva a menor velocidad de conducción auricular y mayor susceptibilidad al inicio de la fibrilación por extrasistolia auricular o estimulación programada 15. Por otro lado, la evidencia mostrada en relación a la disminución de episodios de FA, tras el aislamiento eléctrico de las venas pulmonares, indica el papel evidente de estas no solo como mecanismo disparador, sino también perpetuador 11.
Mecanismo perpetuadores. — Entre estos se encuentran la descarga continua del foco disparador y/o la re- modelación eléctrica y estructural en la aurícula, que se caracteriza por dilatación auricular, acortamiento de los periodos refractarios, dispersión de la refractariedad, presencia de conducción atrial inhomogénea con aparición de zonas de bloqueo, conducción lenta y la disociación eléctrica entre diferentes músculos atriales. Esta remodelación eléctrica puede estar presente desde el inicio, pero, en general, es el resultado de episodios repetidos, de forma tal que la fibrilación auricular genera más fibrilación auricular. La característica anatómica principal de esta remodelación atrial es la dilatación, acompañada por un incremento progresivo en la fibrosis intersticial, el miocardio fibrótico se caracteriza por distorsión y frecuencia de las uniones intercelulares, alteraciones en el acoplamiento intercelular con aparición de múltiples circuitos en zigzag. Precisamente, estas alteraciones estructuras combinadas con los cambios electrofisiológicos constituyen el sustrato perfecto para la perpetuación de la FA.15
Tratamiento
El tratamiento de la FA abarca tres pilares fundamentales:
• Prevención de ACV cardioembólico.
• Control del ritmo cardiaco.
• Control de la frecuencia cardíaca.
Prevención de ACV y embolias sistémicas
Como ya se ha mencionado, la FA aumenta de forma exponencial el riesgo de sufrir un accidente cerebrovascular (ACV), este riesgo es individual y para determinarlo se han desarrollado varios esquemas de estratificación, el más utilizado es el esquema CHA2DS2 – VASc (tabla 1), implementado en el año 2010 por la Sociedad Europea de Cardiología, en el cual, mediante una puntuación de entre 1-9, se estima el riesgo anual de presentar un ACV (tabla 2),16 y todos los pacientes con puntuación igual o mayor a 2 tienen criterio establecido de recibir anticoagulación oral.
Tabla 1.- Escala de puntuación de riesgo embólico CHA2DS2 – VASc
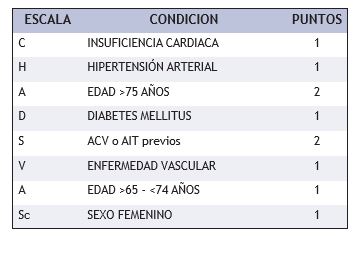
Tabla 2.- Riesgo de ACV según puntuación CHA2DS2 – VASc

La efectividad de la anticoagulación está muy bien de- mostrada, es así que los ensayos clínicos que comparaban la eficacia de la anticoagulación con dicumarínicos frente al ácido acetilsalicílico (ASS), o frente a placebo, se vieron en la necesidad de suspenderse prematuramente por el aumento de incidencia de ACV en el grupo placebo 17,18 y los datos respecto a la ASS respaldan su desuso para este objetivo en la práctica clínica, ya que no se demuestra la reducción del ictus y sí un aumento importante del riesgo del sangrado mayor 19.
Opciones de anticuagulación
DICUMARÍNICOS. — Los medicamentos antagonistas de la vitamina K (Warfarina/Acenocumarol) han demostrado una reducción del riesgo de ACV en un 64% y la mor- talidad en un 26% 20, y se mantienen como fármaco de elección en pacientes con estenosis mitral reumática o portadores de prótesis valvular mecánica; su principal inconveniente es la dificultad de estabilizar su rango terapéutico y las múltiples interacciones que presentan y que pueden alterar la intensidad de su efecto anticoagulante, por lo tanto, su acción de protección; por todo esto, su uso ha disminuido con la llegada de los nuevos anticoagulantes orales.
NUEVOS ANTICOAGULANTES ORALES. — Sus exponentes son el Apixaban, Edoxaban, Rivaroxaban y Dabigatran son anticoagulantes no dependientes de la vitamina K y, en los estudios comparativos con Warfarina, demostraron no inferioridad con menor tasa de eventos hemorrágicos y reducción adicional de la mortalidad. La estabilidad plasmática, seguridad y mejor predicción dosis/respuesta los han convertido en los medicamentos de elección para la prevención de ACV en FA 21.
En conclusión, la anticoagulación crónica deben recibirla todos los pacientes con FA independientemente de su presentación (paroxística, persistente o permanente) e incluso si el paciente se encuentra en ritmo sinusal, pero cumple con riesgo alto de ACV según las escalas de estratificación, la anticoagulación es segura en ancianos y deben recibirla, las contraindicaciones absolutas son escasas: hemorragia activa grave, trombocitopenia grave (plaquetas <50.000) o anemia grave en estudio. Los nuevos anticoagulantes son los medicamentos que mejor perfil de seguridad/eficacia presentan, sin embargo, en ausencia de estos, los dicumarínicos continúan siendo una opción válida con seguimiento adecuado y, por último, la ASS debe descontinuarse como tratamiento preventivo de ictus.
Control del ritmo cardíaco
CARDIOVERSIÓN
La cardioversión se realiza bajo dos escenarios funda- mentales: uno es el paciente hemodinámicamente estable, que nos permite un mayor margen tanto para la elección del método como para el momento de aplicar- lo, y otro muy diferente es el paciente hemodinámica- mente inestable; en este segundo caso, la actuación ha de ser inmediata y la cardioversión eléctrica sincroniza- da es el método de elección, ya que es más efectiva que la farmacológica. La estrategia de alta potencia fija ha mostrado mejores resultados que cargas crecientes de energía. En el otro extremo está el paciente estable que requiere una cardioversión electiva, bajo estas circunstancias puede plantearse el uso de fármacos antiarrítmicos (FAA), que, si bien tiene una menor efectividad, no requiere el uso de sedación, además de que pueden administrarse antes de la cardioversión eléctrica a fin de facilitarla 22,23.
En paciente con escasos episodios de FA paroxística, la estrategia de “pastilla en el bolsillo” puede ser válida sobre todo con el uso de antiarrítmicos clase IC, como la flecainida y la propafenona, siempre y cuando la seguridad y efectividad del fármaco haya sido probada previa- mente en el ámbito hospitalario 24.
La elección del FAA para el uso agudo o de mantenimiento dependerá fundamentalmente del tipo y la gravedad de la cardiopatía asociada. La flecainida y otros fármacos IC se emplean en ausencia de hipertrofia ventricular izquierda significativa, disfunción ventricular sistólica o cardiopatía isquémica con efectividad entre 3 a 5 horas tras su administración. La amiodarona, si bien es menos efectiva de forma aguda, se puede emplear en aquellos pacientes para los que no son una opción los antiarrítmicos IC 25. El vernakalant intravenoso es el más efectivo y de más rápido efecto, puede emplearse en paciente con insuficiencia cardiaca leve y/o cardiopatía isquémica, no hay presentación oral 26.
Ha de señalarse que la espera y vigilancia del paciente puede resultar útil, ya que entre un 76-83% de pacientes con FA de novo puede revertir espontáneamente en las primeras 48 horas, por lo que esta estrategia es válida como alternativa a la cardioversión temprana 27.
ABLACIÓN.
La ablación con catéter de la FA es un tratamiento completamente establecido para el tratamiento de la FA y la prevención de recurrencias. Se trata de una intervención segura y con mejores resultados que el empleo de FAA, tanto para mantener el ritmo sinusal como para la mejo- ría de los síntomas 28, 29.
El tratamiento ablativo de la FA tiene como estrategia fundamental el aislamiento eléctrico de las venas pulmonares. Actualmente se realiza mediante dos modalidades fundamentales: la crioablación y la aplicación de radiofrecuencia. No obstante, es un abordaje en constante desarrollo, al día de hoy se estudian diferentes tecnologías como aplicación de energía láser, calor pul- sado, alcohol, combinación de navegación tridimensional y crioablación, neuroablación, entre otras.
Si bien el tratamiento ablativo aún no es la solución definitiva para la resolución de esta entidad, el aislamiento eléctrico de las venas pulmonares constituye en la actualidad la modalidad terapéutica con mejores resulta- dos 1. Hay dos factores que se relacionan directamente con ello, por un lado, la evolución de las herramientas, evolución de tecnología de catéteres, nuevos balones, softwares,
etc., y, por otro, la indicación de intervención con indicación cada vez más precoz 30-33. A este respecto, el reciente estudio de Paulus Kirchhof et al. demostró que los pacientes con estrategia de control precoz de ritmo tenían mejor evolución, menor mortalidad, menor incidencia de ictus, menor número de ingreso por empeoramiento de insuficiencia cardiaca o síndrome coronario agudo 31.
La ablación de la FA es efectiva para el mantenimiento del ritmo sinusal, tanto en la presentación paroxística como en la persistente. Entre los beneficios clínicos más importantes se encuentra la reducción de la sintomatología relacionada con la arritmia, lo que quedó demostrado en el reciente estudio aleatorizado de Blomstrom-Lundqvist C 32, con mejores resultados en calidad de vida y en carga arrítmica, así también se confirmó en el estudio CABANA 29 en donde los pacientes derivados a ablación de FA presentaron menor incidencia de muerte, ACV y hospitalización por falla cardiaca comparado con el tratamiento farmacológico solo.
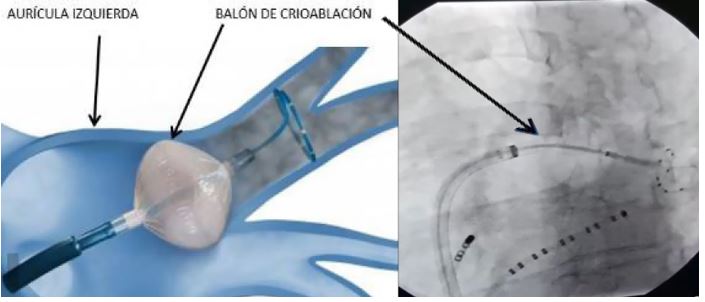
Como describíamos anteriormente, el aislamiento eléctrico de las venas pulmonares (AVP) constituye la piedra angular del tratamiento ablativo. Este objetivo se obtie-ne mediante la aplicación de calor en forma de radiofre-cuencia por fuera de la zona antral de las venas, creando una circunferencia de lesiones punto a punto, que se realiza apoyado en un sistema de navegación tridimensional y el uso de catéteres de ablación irrigados con medición de la fuerza de contacto; la figura 2 muestra un ejemplo de este procedimiento. Otro de los métodos más empleados para el AVP es la crioablación, que se trata de la inyección de una sustancia refrigerante a través de un criobalón que se inserta en la región antral de las venas pulmonares, figura 3. El estudio FIRE AND ICE34 comparó ambas técnicas demostrando no inferioridad de la crioablación, incluso ciertos beneficios de esta en cuanto a menor tiempo de procedimiento, menor hospitalización y recurrencias postprocedimiento. Ambas intervenciones tienen una efectividad superior al 70%, con tasa de complicaciones entre el 2-5% 35. Actualmente se espera los resultados del estudio EAST que aportará datos importantes sobre el impacto de la ablación en los eventos cardiovasculares.
Figura 2.- Ejemplo de aislamiento de venas pulmonares guiada por Mapeo Tridimensional.

Referencias
- Gerhard Hindricks, Tatjana Potpara, Nikolaos Dagres et al. 2020 ESC Guidelines for the di- agnosis and management of atrial fibrillation developed in collaboration with the European Association of Cardio-Thoracic Surgery (EACTS). Eur Heart J. 2020 Aug 29; ehaa612. doi: 10.1093/eurheartj/ehaa612
- Kim MH, Johnston SS, Chu BC, et al. Estimation of total incremental health care costs in patients with atrial fibrillation in the United States. Circ Cardiovasc Qual Outcomes. 2011; 4:313–320. https://doi.org/10.1161/CIRCOUTCOMES.110.958165
- Nicole Lowres, Lis Neubeck, Julie Redfern et al. Screening to identify unknown atrial fibril- A systematic review. Thromb Haemost 2013; 110(02): 213-222. https://doi.org/10.1160/TH13-02-0165
- Chugh SS, Havmoeller R, Narayanan K, et Worldwide epidemiology of atrial fibrillation: a Global Burden of Disease 2010 Study. Circulation. 2014; 129:837–847. https://doi.org/10.1161/CIRCULATIONAHA.113.005119
- Stewart S, Murphy NF, Walker A, et Cost of an emerging epidemic: An economic analysis of atrial fibrillation in the uk. Heart. 2004; 90:286–292. https://doi.org/10.1136/hrt.2002.008748
- Lee WC, Lamas GA, Balu S, et al. Direct treatment cost of atrial fibrillation in the elderly american population: A medicare J Med Econ. 2008; 11:281–298. https://doi.org/10.1185/136969908X312151
- Kim MH, Johnston SS, Chu BC, Dalal MR, et al. Estimation of total incremental health care costs in patients with atrial fibrillation in the united Circ Cardiovasc Qual Outcomes. 2011; 4:313–320. https://doi.org/10.1161/CIRCOUTCOMES.110.958165
- Macle L, Cairns J, Leblanc K, et 2016 Focused Update of the Canadian Cardiovascu- lar Society Guidelines for the Management of Atrial Fibrillation. Can J Cardiol. 2016 Oct;32(10):1170-85. https://doi.org/10.1016/j.cjca.2016.07.591
- Chinitz JS, Vaishnava P, Narayan RL, Fuster Atrial fibrillation through the years: contempo- rary evaluation and management. Circulation. 2013 Jan;127(3):408-16. https://doi.org/10.1161/CIRCULATIONAHA.112.115196
- Emelia J Benjamin, Peng-Sheng Chen, Diane E Bild et al. Prevention of atrial fibrillation: report from a national heart, lung, and blood institute 2009 Feb 3; 119(4):606-18. 10.1161/CIRCULATIONAHA.108.825380
- Haissaguerre, P. Sanders, M. Hocini, et al . Pulmonary veins in the substrate for atrial fibrillation: the “venous wave” hypothesis. J Am Coll Cardiol., 43 (2004), pp. 2290-2292. https://doi.org/10.1016/j.jacc.2004.03.024
- Sanchez-Quintana, J.A. Cabrera, V. Climent, et al.How close are the phrenic nerves to cardiac structures?. Implications for cardiac interventionalists. J Cardiovasc Electrophysiol., 16 (2005), pp. 309-313. https://doi.org/10.1111/j.1540-8167.2005.40729.x
- Morphological evidence of muscular connections between continuous pulmonary venous or- ifices: relevance of the interpulmonary isthmus for catheter ablation in atrial fibrillation. Heart , 6 (2009), pp. 1192-1198. https://doi.org/10.1136/hrt.2008.157834
- I. Yeh, Y.J. Lai, S.H. Lee, et al. Heterogeneity of myocardial sleeve morphology and gap junctions in canine superior vena cava. Circulation., 104 (2001), pp. 3152-3157. https://doi.org/10.1161/hc5001.100782
- Jais, M. Hocini, L. Macle, et al. Distinctive electrophysiological properties of pulmonary veins in patients with atrial fibrillation. Circulation., 106 (2002), pp. 2479-2485. https://doi.org/10.1161/01.CIR.0000036987.46510.89
- Camm, John; Lip, Gregory Y. H.; De Caterina, Raffaele; et al 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: an update of the 2010 ESC Guide- lines for the management of atrial fibrillation. Developed with the special contribution of the European Heart Rhythm Association. European Heart Journal 33 (21): 2719-2747. https://doi.org/10.1093/eurheartj/ehs253
- S J Connolly 1, A Laupacis, M Gent, et al. Canadian Atrial Fibrillation Anticoagulation (CAFA) J Am Coll Cardiol. 1991 Aug;18(2):349-55. doi: 10.1016/0735-1097(91)90585-w
- D E Singer 1, R A Hughes, D R Gress et al. The effect of aspirin on the risk of stroke in patients with nonrheumatic atrial fibrillation: The BAATAF Am Heart J. 1992 Dec;124(6):1567- 73. 10.1016/0002-8703(92)90074-6
- Mant J, Hobbs FD, Fletcher K, Roalfe A, et al. BAFTA investigators, Midland Research Practic- es Network (MidReC). Warfarin versus aspirin for Stroke prevention in an elderly community population with atrial fibrillation (the Birmingham Atrial Fibrillation Treatment of the Aged BAFTA): a randomised controlled trial. Lancet. 2007; 370:493–503. https://doi.org/10.1016/S0140-6736(07)61233-1
- Hart RG, Pearce LA, Aguilar MI. Meta-analysis: antithrombotic therapy to prevent Stroke in patients who have nonvalvular atrial Ann Intern Med. 2007; 146:857–867. https://doi.org/10.7326/0003-4819-146-12-200706190-00007
- Ruff CT, Giugliano RP, Braunwald E, et al. Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation: a meta-analysis of ran- domised Lancet. 2014;383:955–962. https://doi.org/10.1016/S0140-6736(13)62343-0
- Um KJ, McIntyre WF, Healey JS, Mendoza PA, Koziarz A, Amit G, Chu VA, Whitlock RP, Bel- ley-Cote EP. Pre- and post-treatment with amiodarone for elective electrical cardioversion of atrial fibrillation: a systematic review and meta-analysis. 2019; 21:856–863. https://doi.org/10.1093/europace/euy299
- Kirchhof P, Monnig G, Wasmer K, Heinecke A, Breithardt G, Eckardt L, Bocker D. Atrial of self-adhesive patch electrodes and hand-held paddle electrodes forexternal cardioversion of atrial fibrillation (MOBIPAPA).Eur Heart 2005;26:1292–1297. https://doi.org/10.1093/eurheartj/ehi156
- Dan GA, Martinez-Rubio A, Agewall S, Boriani G, Borggrefe M, Gaita F, et al. ESC Scientific Doc- ument Group. Antiarrhythmic drugs-clinical use and clinical decision mak-ing: a consensus doc- ument from the European Heart Rhythm Association (EHRA) and European Society of Cardiolo- gy (ESC) Working Group on CardiovascularPharmacology, endorsed by the Heart Rhythm Society (HRS), Asia-Pacific HeartRhythm Society (APHRS) and International Society of Cardiovascular Pharmaco-therapy (ISCP).Europace.2018;20:731–732. https://doi.org/10.1093/europace/eux373
- Markey GC, Salter N, Ryan J. Intravenous flecainide for emergency department management of acute atrial J Emerg Med.2018;54:320–327. https://doi.org/10.1016/j.jemermed.2017.10.007
- Pohjantahti-Maaroos H, Hyppola H, Lekkala M, et al. Intravenous vernakalant in comparison with intravenous flecainide in the cardioversion of recent-onset atrial fibrillation. Eur Heart J Acute Cardiovasc 2019;8:114–120. https://doi.org/10.1177/2048872617702505
- Pluymaekers N, Dudink E, Luermans J, et al. RACE ACWAS Investigators Early or delayed cardio- version in recent-onset atrial N Engl J Med.2019;380:1499–1508. https://doi.org/10.1056/NEJMoa1900323
- Chen C, Zhou X, Zhu M, Chen S, et al. Catheter ablationversus medical therapy for patients with persistent atrial fibrillation: asystematicreview and meta-analysis of evidence from randomized J IntervCard Electrophysiol. 2018; 52:9–18.617. https://doi.org/10.1007/s10840-018-0326-0
- Packer DL, Mark DB, Robb RA, et al. CABANA Investigators. Effect of catheter ablation vs an- tiar-rhythmic drug therapy on mortality, stroke, bleeding, and cardiac arrest amongpatients with atrial fibrillation: the CABANA randomized clinical JAMA.2019;321:1261–1274. https://doi.org/10.1001/jama.2019.0693
- Bisbal F., Mont LL., Ferreo A. et al. Tiempo del diagnóstico a la ablación de fibrilación auricular: un parámetro modificable asociado al pronóstico. Rev Esp 2017;70 (Supl 1):333. https://doi.org/10.1016/j.recesp.2016.10.022
- Paulus Kirchhof, A John Camm, Andreas Goette, et al. EAST-AFNET 4 Trial Investigators. Early Rhythm-Control Therapy in Patients with Atrial Fibrillation. N Engl J Med. 2020 Aug 29. Online ahead of print. https://doi.org/10.1056/NEJMoa2019422
- Blomstrom-Lundqvist C, Gizurarson S, Schwieler J, et al. Effect of catheter ablation vs antiar- rhythmic medication on quality of life in patients with atrial fibrillation: the CAPTAF randomized clinical JAMA. 2019;321:1059–1068. https://doi.org/10.1001/jama.2019.1183
- Kirchhof P, Breithardt G, Camm AJ, et al. Improving outcomes in patients with atrial fibrillation: rationale and design ofthe Early treatment of Atrial fibrillation for Stroke prevention Trial. Am Hear 2013;166:442–448. https://doi.org/10.1016/j.ahj.2013.05.002
- Kuck KH, Brugada J, Fürnkranz A, el ; FIRE AND ICE Investigators. Cryoballoon or radiofrequen- cy ablation for paroxysmal atrial fibrillation. N Engl J Med. 2016; 374:2235–2245. https://doi.org/10.1056/NEJMoa1602014
- Roberto Keegan, Luis Aguinaga, Nicolás Valera, et al. Catheter ablation of atrial fibrillation in Latin America: results of the first registry of the Latin American Society of Pacing and Electro- physiology Cardiac (SOLAECE). Revista Uruguaya de Cardiología, vol. 31, núm. 1, pp. 165-175, 2016. Ver en Scielo
Cómo citar el presente artículo:
Apolo J, Alemán A. Fibrilación auricular: de arritmia infradiagnosticada a epidemia cardiológica. Revisión Bibliográfica. Indexia. Abril 2022.
Todos los artículos se publican bajo la licencia Creative Commons Atribución 4.0 Internacional (CC-BY 4.0), lo que permite compartir y adaptar el contenido siempre que se dé el crédito adecuado a los autores y a la revista.
