REVISIÓN BIBLIOGRÁFICA

Cannabis medicinal como parte de la oncología integrativa
Medicinal Cannabis as part of Integrative Oncology
Dra. Yannely Carolina Polanco Contreras 1 2 3
- Carrera de Médico Cirujano, Universidad del Zulia, Venezuela.
- Especialidad Radioterapia y Medicina Nuclear, Instituto Autónomo Hospital Universitario de Caracas, Venezuela.
- Diplomado Internacional Uso Terapéutico del Cannabis Medicinal, Universidad de Las Américas, Ecuador
Palabras Clave:Oncología integrativa, cannabis, cannabinoides, soporte, paliación
Keywords: Integrative Oncology, Cannabis, Cannabinoids, support, palliation
Fecha recepción: 29-06-2024
Fecha aceptación: 06-08-2024
Fecha publicación: 22-10-2024
DOI: 10.65183/revind.e12.05
Resumen
La oncología integrativa es un enfoque holístico del tratamiento del cáncer, que combina terapias convencionales con enfoques complementarios y alternativos para mejorar la calidad de vida del paciente que atraviesa por esta enfermedad. El cannabis medicinal es una de las opciones más investigadas y utilizadas; a pesar de su legalización, aún es tema de debate en muchos países. En esta publicación se busca reflejar mediante una revisión bibliográfica evidencias científicas de los múltiples componentes de su extracto, siendo los más conocidos el 9-tetrahidrocannabinol, de efectos psicoactivos, y el cannabidiol, de efectos no psicoactivos, cómo estos interactúan con el sistema endocannabinoide de mamíferos, que juega un papel en la regulación de diversas funciones, incluyendo dolor, inflamación, apetito, estado de ánimo y sueño, lo que ha llevado al desarrollo de fármacos tanto sintéticos como de extractos altamente purificados de la planta, con aprobación de la Administración de Alimentos y Medicamentos de los Estados Unidos para su uso en patologías específicas. Sin embargo, el uso potencial para sintomatología de la enfermedad oncológica, así como efectos secundarios o secuelas del tratamiento, lo hacen una herramienta de soporte para pacientes y supervivientes de cáncer aceptable, de creciente demanda, reflejada en el desarrollo de directrices internacionales que orientan al personal de salud en cuanto a recomendaciones para el uso asertivo y responsable de esta planta milenaria.
Summary
Integrative oncology is a holistic approach to cancer treatment that combines conventional therapies with complementary and alternative approaches to improve the quality of life of the patient experiencing this disease. Medical cannabis is one of the most researched and used options, despite its legalization still being a topic of debate in many countries. This publication seeks to reflect, through a bibliographic review, scientific evidence of the multiple components of its extract, the best known being 9-tetrahydrocannabinol with psychoactive effects and cannabidiol with non-psychoactive effects, how these interact with the mammalian endocannabinoid system, which plays a role in regulating various functions, including pain, inflammation, appetite, mood and sleep. Which has led to the development of both synthetic drugs and highly purified extracts of the plant with approval from the United States Food and Drug Administration for use in specific pathologies. However, the potential use for symptoms of the oncological disease as well as side effects or sequelae of the treatment, make it an acceptable support tool for cancer patients and survivors, with increasing demand, reflected in the development of international guidelines that guide personnel of health regarding recommendations for the assertive and responsible use of this ancient plant.
Introducción
La medicina integrativa es un enfoque de terapias complementarias y alternativas para brindar una atención integral a los pacientes. Sus raíces se remontan a las antiguas prácticas, como medicina china, el ayurveda y la medicina indígena americana, así como el enfoque holístico de la salud, considerando la mente, el cuerpo y el espíritu como un todo. Su acreditación en Estados Unidos desde el año de 1992 con la creación de un apartado de investigación llamado Oficina de Medicina Alternativa, dependiente del Instituto Nacional de Salud, dio paso a la investigación y consecuente enfoque basado en evidencias. Posteriormente, en 1998, se le otorga una posición como departamento independiente, cambiando su nominación a Centro Nacional de Medicina Complementaria y Alternativa, que permitió el inicio de creación de publicaciones y directrices, que dieron lugar a la aceptación de estas terapias. Finalmente, en 2014, el congreso renombra al Centro Nacional de Salud Complementaria e Integrativa, como es conocido hasta la fecha, proporcionando estudios de investigación rigurosos, que agrupan estadísticas nacionales e internacionales del beneficio y seguridad, que avalan el uso de la medicina complementaria 1.
Por otra parte, la aplicación de terapias complementarias en el área oncológica ha ganado reconocimiento como una opción prometedora para mejorar la calidad de vida, el manejo de los síntomas y la reducción de los efectos secundarios del tratamiento del cáncer. Desde 1990 se han desarrollado centros bimodales en conjunto con los tratamientos convencionales. Con el establecimiento en 2003 de la Sociedad de Oncología Integrativa (SIO) (Estados Unidos), una organización profesional multidisciplinaria sin fines de lucro, el término “oncología integrativa” se legitimó aún más y comenzó a ser ampliamente utilizado 2. Las directrices de práctica clínica de SIO tienen referencias en MedLine y están publicadas en el sitio web del Centro Nacional de Salud Complementaria e Integrativa de los Institutos Nacionales de Salud. Estas guías integrales, basadas en evidencia, tienen el objetivo de incorporar terapias complementarias e inclusivas en la práctica clínica de oncología convencional, las cuales están disponibles sin costo alguno 3.
Desde el año 1500 antes de Cristo, el cannabis ha sido descrito para variedad de dolencias, como dolor, inflamación, espasmos musculares y problemas digestivos. En el siglo XVIII, Carolus Linnaeus creó un sistema formalizado de clasificación de organismos vivos basado en sus relaciones anatómicas, que conocemos como nomenclatura taxonómica. Históricamente, el género Cannabis ha sido descrito de tres formas bajo este sistema: Cannabis sativa, por C. Linnaeus en 1753; Cannabis indica, por J.B. Lamarck en 1785; y Cannabis ruderalis, por D. E. Janischewsky en 1924; derivadas estas clasificaciones taxonómicas de características físicas, morfológicas, químicas y datos geográficos. Si bien los métodos morfológicos y fenotípicos han tenido éxito para muchas especies, han resultado inadecuados para resolver la clasificación de ciertas especies, como el Cannabis. Sin embargo, el uso de herramientas y técnicas genómicas ha permitido a los investigadores identificar variaciones genéticas, diferenciar entre especies y subespecies debido a la polinización por el viento, la naturaleza heterocigótica de las plantas, actuales prácticas de cultivo y una domesticación incompleta, junto con pedigríes reproductivos mal rastreados. El 9-tetrahidrocannabinol (THC) es el principal cannabinoide psicoactivo a partir de las flores femeninas de la planta, aquellas con menos de 0,3% de THC se clasifican como cáñamo, mientras que las plantas que producen 0,3% o más de THC se clasifican como tipo droga sujeta a fiscalización 4. No obstante, la planta produce más de 120 tipos diferentes de cannabinoides.
Otros de ellos, importantes por su interés médico, son el cannabidiol (CBD), el cannabinol (CBN), el cannabicromeno (CBC) y el cannabigerol (CBG), cada uno con efectos distintos descritos, pero que, en conjunto con el compuesto aromático básico de las plantas llamado terpenos, como el mirceno, el limoneno, el linalool, el beta-cariofileno y el pineno, hacen un “efecto séquito”. El efecto séquito, también conocido como efecto entourage, es una teoría que propone que los distintos compuestos presentes en la planta de cannabis, como cannabinoides, terpenos y flavonoides, trabajan en conjunto para producir efectos más completos y potentes que cuando se consumen de forma aislada, sin información concluyente hasta la fecha 5.
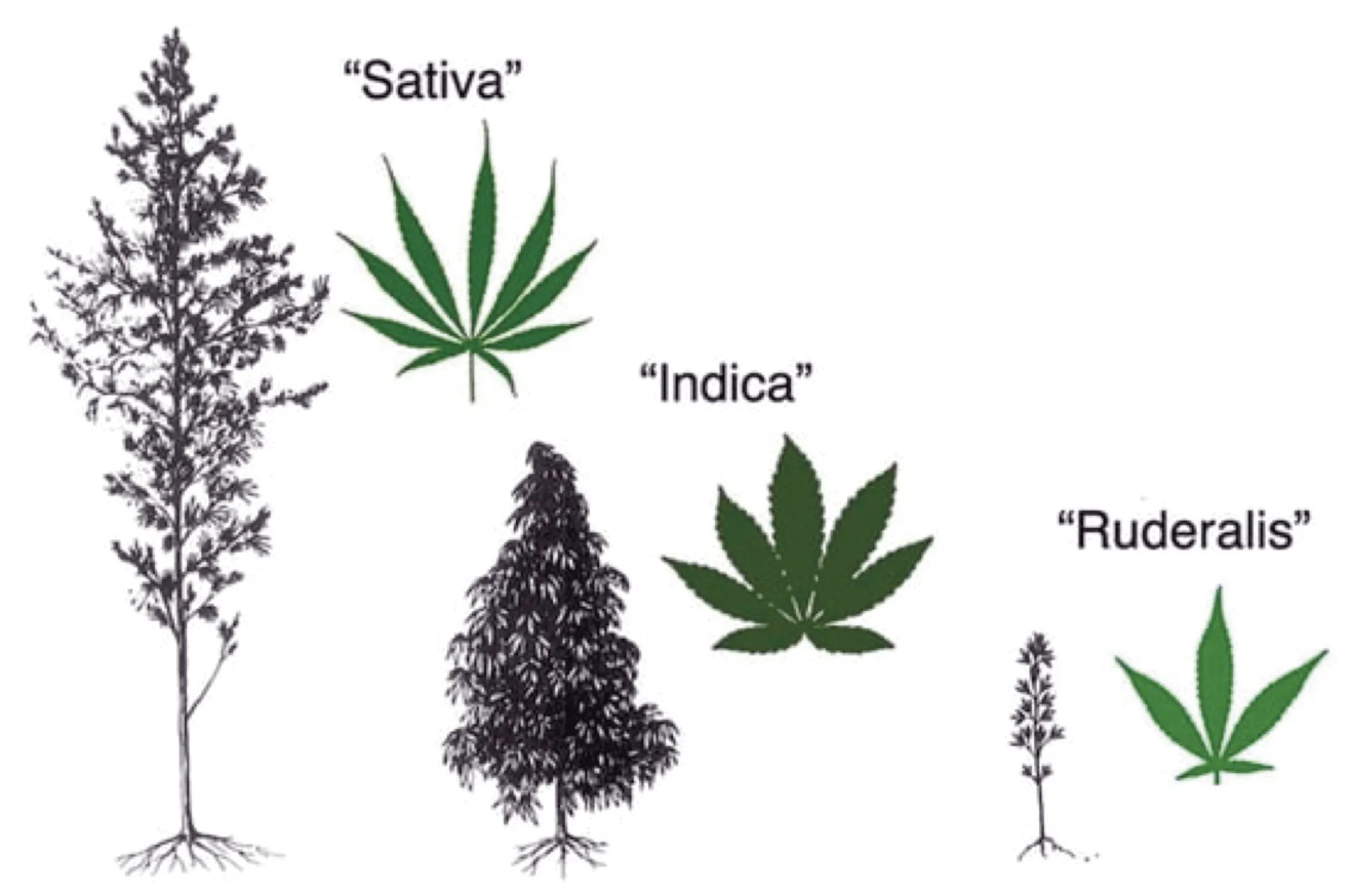
Figura 1. Diferencias morfológicas entre variedades de especies de Cannabis sativa, imagen de John M. McPartland. Investigación sobre cannabis y cannabinoides. Dec 2018.203-212. http://doi.org/10.1089/can.2018.0039.
El cannabis ha tenido una presencia intermitente en las farmacopeas a lo largo de la historia. Las farmacopeas son publicadas por autoridades sanitarias, como la Organización Mundial de la Salud (OMS) o la Agencia Europea de Medicamentos (EMA), y son de obligado cumplimiento para los fabricantes, con el objetivo de garantizar la calidad y seguridad de los medicamentos.
No fue sino hasta el siglo XIX que se incluyó en las farmacopeas de varios países, como Estados Unidos y Gran Bretaña 6. Sin embargo, en la década de 1920, se firmaron diferentes convenciones internacionales que restringían el uso del cannabis, entre otras sustancias, como la Convención Internacional del Opio de 1925, firmada en Ginebra, y la Convención Única de Estupefacientes de 1961, firmada en Nueva York; esta última es el principal tratado que conforma el marco legal internacional para el control de drogas. Una de las disposiciones importantes fue establecer un sistema de control internacional para 133 drogas, clasificadas en cuatro listas según su potencial de abuso y dependencia. Se ubica el cannabis en la lista I, comparándose con opio, heroína, metadona, cocaína, hoja de coca, oxicodona. Como resultado, estas convenciones clasificaron el cannabis como una droga peligrosa, lo que llevó a su prohibición en muchos países, y se limitó su uso médico y científico 7. En este sentido, se han planteado propuestas para reformar la Convención de 1961, con el fin de flexibilizar las restricciones impuestas al cannabis y permitir un mayor acceso a sus usos medicinales. Al mismo tiempo, la evidencia científica sobre los beneficios medicinales plantea un desafío a la clasificación actual de esta sustancia como una droga altamente peligrosa, puesto que la prohibición absoluta del cannabis ha generado un mercado negro lucrativo y violento, lo que ha tenido un impacto negativo en la salud pública y la seguridad.
Convención Única sobre Estupefacientes de 1961
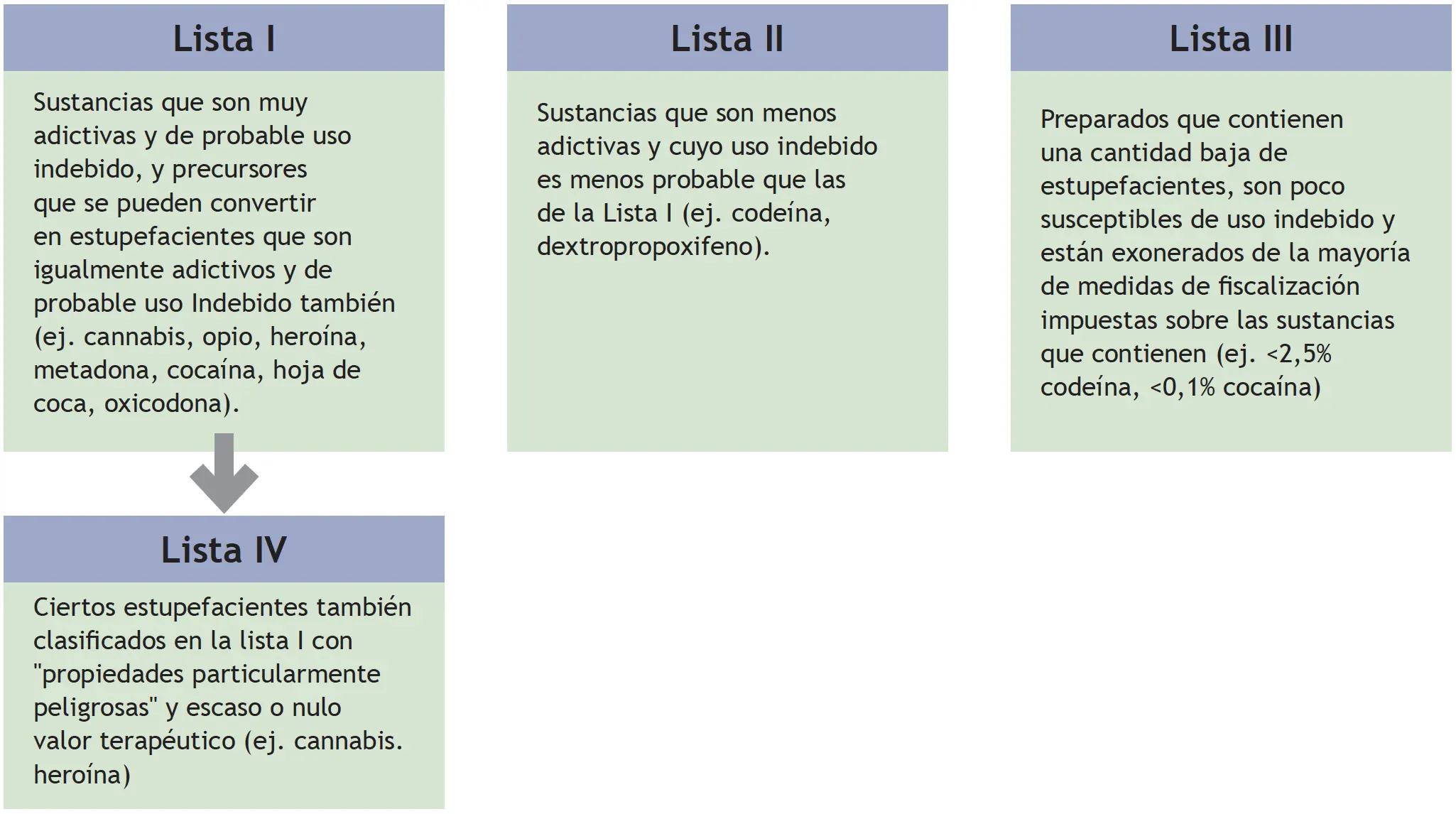
Figura 2. Listas de Fiscalización de Estupefacientes de la Organización de Naciones Unidas (ONU), según convención 1961, vigente hasta la fecha.
Las publicaciones con evidencia científica datan de 1988 cuando se determina y caracteriza la existencia de receptor cannabinoide en el cerebro de ratas, denominado CB18. Posteriormente, en 1993, un segundo receptor justificó la investigación sobre efectos y posibles usos de esta unión receptor-ligando representado por los cannabinoides derivados de la planta, desarrollando toda una nueva fisiología en el sistema de mamíferos y consecuente fisiopatología. Este avance permitió diferenciar la presencia predominante del receptor CB1 en sistema nervioso central versus la presencia de receptores en tejidos periféricos como células inmunitarias, específicamente macrófagos del bazo, nombrándose receptor CB2. Esto llevo a la conclusión de que los cannabinoides pueden, entonces, tener efectos psicoactivos y no psicoactivos 9.
Históricamente, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) no aprueba el uso de la planta del cannabis como un todo para el uso terapéutico, no obstante, debido a la evidencia científica de soporte, en 1985 esta institución aprueba el dronabinol, un 9-tetrahidrocannabinol sintético (THC), para el tratamiento de la anorexia inducida por el virus de inmunodeficiencia humana/síndrome inmunodeficiencia adquirida, las náuseas y vómitos inducidos por la quimioterapia en pacientes que no han respondido a los antieméticos convencionales. Por su parte, el Departamento de Justicia y Administración de Control de Drogas (DEA) lo ubica en la clasificación II de la Ley de Sustancias Controladas, con un alto potencial de abuso10.
Además, publicaciones claves en revistas científicas reconocidas como Science, en 1992, por Devane y sus colaboradores, condujeron a la identificación y caracterización de la N-araquidonoiletanolamida, más adelante denominada anandamida, demostrando que fue aislada del tejido cerebral porcino. Por lo que es sintetizada de forma endógena, exhibió una alta afinidad de unión a los receptores cannabinoides, ratificando el conocimiento de receptores y ampliando a ligandos no solamente externos, sino internos. La anandamida produce efectos similares a los cannabinoides externos, describiéndose efectos farmacológicos similares a los del THC, como la inhibición de la liberación de neurotransmisores. Este descubrimiento sentó las bases para investigaciones posteriores sobre el sistema endocannabinoide, incluyendo la identificación de endocannabinoides adicionales, la caracterización de sus vías biosintéticas y la exploración de sus roles en diversos procesos fisiológicos 11.
En 1997, Pharmacology & Therapeutics, Pertwee describe los aspectos fisiológicos y farmacológicos de los receptores hasta la fecha, indicando que el receptor CB1 se localiza predominantemente en el sistema nervioso central (SNC). Es uno de los receptores acoplados a proteína G (GPCR) más abundantes en el cerebro, se ubica en órganos como la corteza cerebral, hipocampo, ganglios basales, cerebelo, amígdala, hipotálamo, por lo que predomina su efecto psicoactivo. También se encuentra en densidades más bajas en el sistema nervioso periférico, esto es, digestivo, cardiovascular, reproductivo e inmunitario. El receptor CB2, con menor densidad en el sistema nervioso central (SNC), amígdala e hipocampo, predomina en células y órganos del sistema inmunitario (microglia), leucocitos, bazo, tejidos periféricos como hueso, piel, sistema digestivo, reproductivo, corazón y pulmones12. En conjunto, desempeñan un papel importante en la regulación, modulación del dolor, control del movimiento, conducta alimentaria, estado de ánimo, crecimiento óseo, inflamación, neuroprotección y memoria. Otros receptores bajo investigación, también llamados huérfanos, son GPR55, GPR119, GPR18, TRPV, 5-HT1A.
En 2018, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprueba el cannabidiol (CBD) de origen vegetal, altamente purificado por primera vez, con fines terapéuticos para tratar dos tipos específicos de epilepsia: el síndrome de Lennox-Gastaut y el síndrome de Dravet 13. Así mismo, el Departamento de Justicia y Administración de Control de Drogas (DEA) lo ubica en la clasificación V de la Ley de Sustancias Controladas, con bajo potencial de abuso.
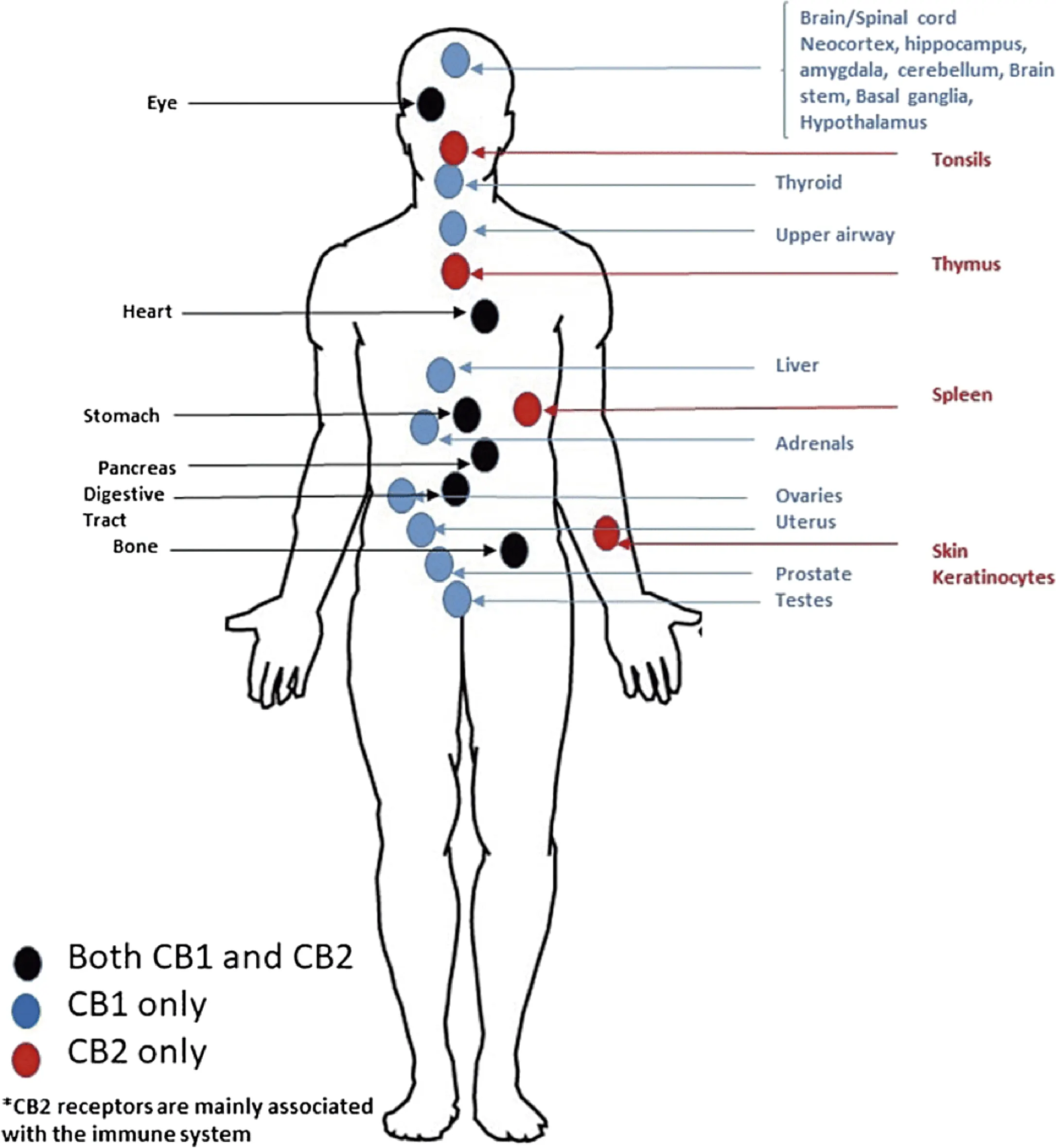
Figura 3. Distribución de receptores cannabinoides en el cuerpo humano, Reddy, P. (2019). Uso medicinal de cannabinoides sintéticos. Una breve revisión. Reportes Actuales de Farmacología. 10.1007/s40495-018-0165-y.
Experiencia latinoamericana
El primer país en Latinoamérica en legalizar el uso medicinal del cannabis fue Chile, en el año 2015. La ley chilena permite el cultivo, producción y venta de cannabis para uso medicinal a través de farmacias autorizadas, reguladas por el Servicio Agrícola y Ganadero (SAG); sin embargo, no han publicado estudios de sus resultados terapéuticos hasta el momento. Desde entonces, otros países han seguido el ejemplo de Chile en el uso medicinal del cannabis, incluyendo Colombia, Argentina, México, Perú, Ecuador, Paraguay, Brasil y Bolivia.
En Ecuador, el uso del cannabis se regula por las siguientes leyes: Ley Orgánica Reformatoria al Código Orgánico Integral Penal (2019): Despenaliza la tenencia o posesión de cannabis no psicoactivo o cáñamo, entendido como la planta de cannabis y cualquier parte de dicha planta, cuyo contenido de delta-9- tetrahidrocannabinol (THC) es inferior a 1% en peso seco, y, de esta forma, se autoriza con fines terapéuticos, paliativos, medicinales o para el ejercicio de la medicina alternativa14. Posterior a este paso, autoridades como la Agencia Nacional de Regulación, Control y Vigilancia Sanitaria (ARCSA), en 2021 emitió y publicó la Normativa Técnica Sanitaria para la regulación y control de productos terminados de uso y consumo humano, que contengan cannabis no psicoactivo o cáñamo, o derivados de cannabis no psicoactivo como el cannabidiol, con la restricción de concentración de THC a menos del 0.3%. Debido a esto, es obligatorio obtener el registro sanitario o la notificación sanitaria obligatoria, que implica la certificación que se expide cuando se cumplen los requisitos de calidad y seguridad para consumir. Actualmente, se regulan presentaciones tipo alimentos procesados, cosméticos y productos medicinales 15.
Con este paso legal indispensable, el crecimiento de la investigación ha permitido el desarrollo de programas educativos en el país, avalados por centros universitarios dirigidos al personal de salud que desea conocer y prescribir asertivamente según la evidencia científica reciente del cannabis medicinal, ya que esta no forma parte de los programas educativos de centros de pregrado en medicina, o especialidades oncológicas.
Metodología
Esta revisión organiza la búsqueda de información obtenida en Pubmed, que incluyó las palabras claves “Marihuana”, “cannabis”, “cáncer”, “oncología integrativa”, “uso medicinal” y “Guideline”, así como publicaciones del Centro Nacional de Salud Complementaria e Integrativa de Estados Unidos. En vista de que existen pocos estudios disponibles, se incluyeron artículos de investigación, difundidos durante el periodo 1979 y el 2018, en idioma inglés. Se excluyeron aquellas publicaciones de muestra menor a 10 pacientes, y el análisis del contenido se llevó a cabo basándose en una clasificación en cuanto al uso de la planta completa versus el uso del extracto de esta para la obtención de un cannabinoide en específico, con mayor concentración. Se realizó síntesis de las ideas y conclusiones relevantes en cada una de ellas.
Tabla 1. Resultados de estudios seleccionados sobre uso de cannabis
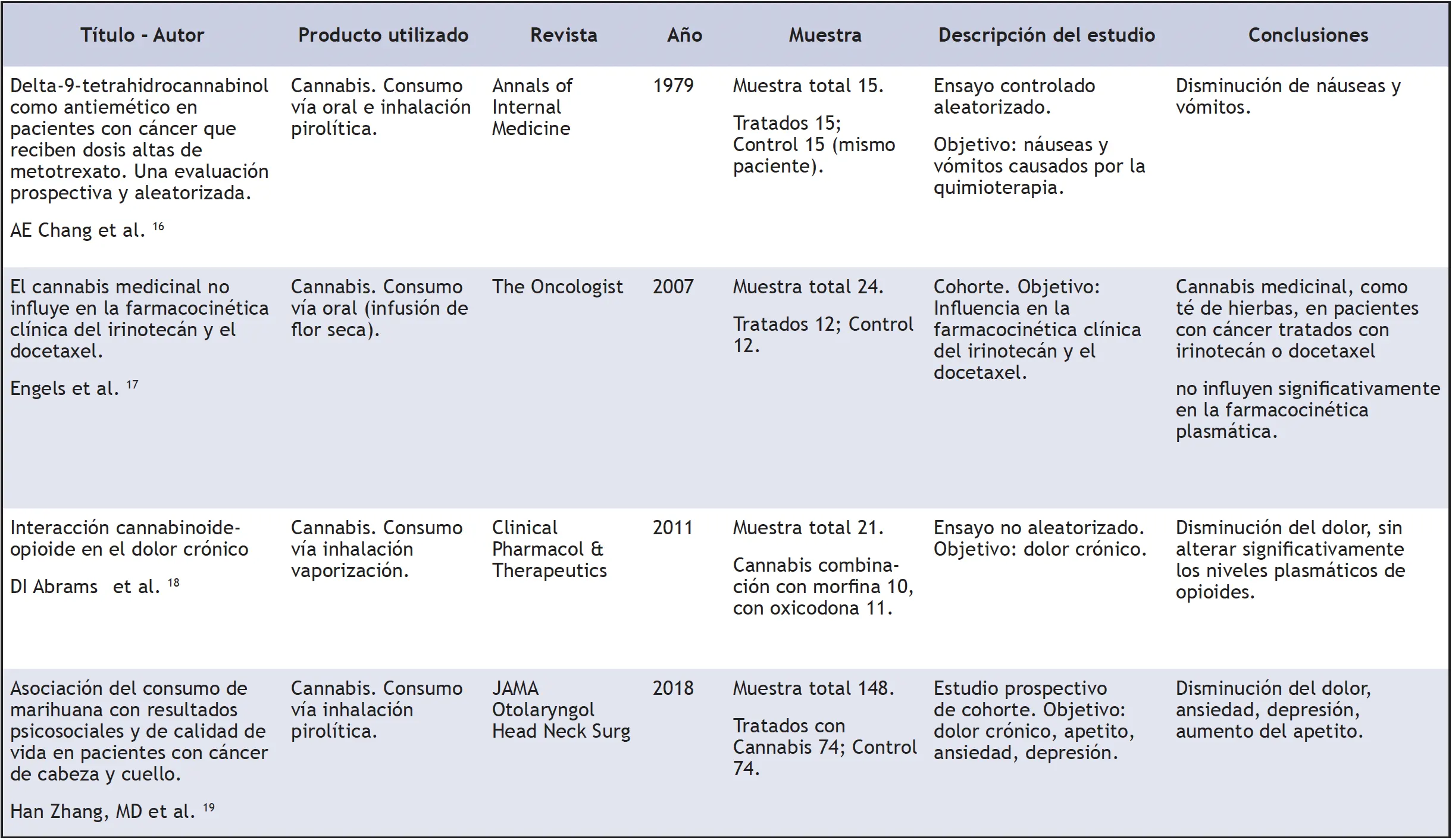
Tabla 2. Resultados de estudios seleccionados sobre uso de cannabinoides
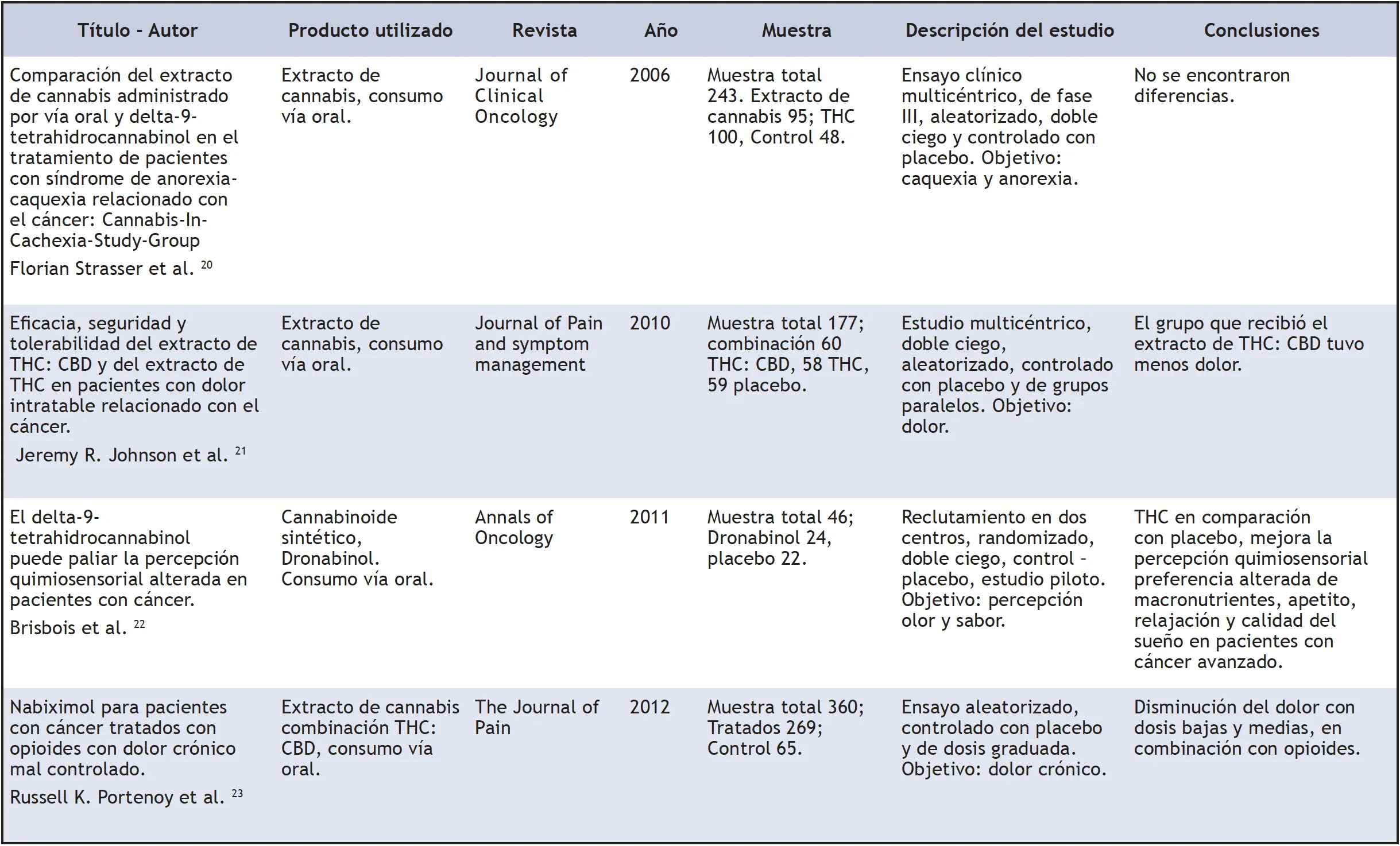
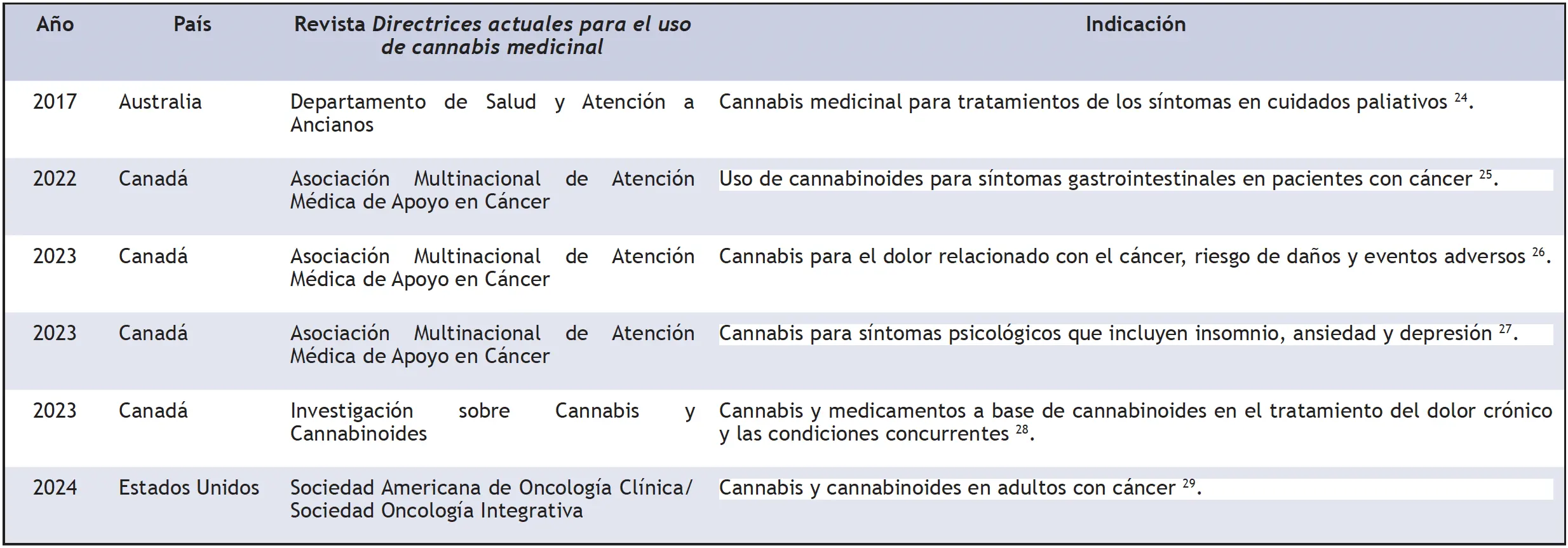
Tabla 3. Directrices actuales para el uso de cannabis medicinal
Discusión y conclusiones
Establecer una práctica de oncología integrativa es una compleja unión de diversos profesionales, que incluye oncólogos clínicos, oncólogos integrativos o médicos con capacitación en terapias complementarias y alternativas, psicooncólogos, enfermeros especializados en oncología, nutricionista en oncología, médicos especialistas en paliación, acupunturista, masajista, terapeuta de yoga e investigadores. El objetivo principal es cerrar la brecha entre la atención convencional del cáncer y las terapias complementarias, fomentando un enfoque centrado en el paciente para abordar los desafíos multifacéticos que enfrentan las personas con esta enfermedad, en pro de mejorar los resultados y las experiencias de estos.
En cuanto a la investigación sobre cannabis y sus derivados, continúan diversas limitaciones que obstaculizan un mayor conocimiento de sus efectos y aplicaciones potenciales. En muchos países, la investigación con cannabis aún está prohibida o sujeta a regulaciones estrictas, lo que limita el número de instituciones y científicos que pueden realizarla. El consumo de cannabis aún está asociado a ciertos estigmas y prejuicios sociales, lo que puede limitar la apertura y la participación en estudios por parte de los individuos. Actualmente, las recomendaciones sobre dosis y vías de administración óptima para cada condición o enfermedad específica es un desafío constante; en muchos casos, no se cuenta con información suficiente sobre la salud y el historial de consumo de cannabis de los participantes en los estudios, lo que dificulta la interpretación de los resultados.
Por otro lado, la investigación sobre los efectos a largo plazo del consumo, tanto positivos como negativos, es aún limitada; a esto agregamos que no existe una estandarización internacional de la planta para fines científicos, lo que genera variabilidad en los resultados. Por ende, los diseños metodológicos sobre la complejidad de los efectos del cannabis y la interacción de sus componentes son limitados al no poderse estructurar análisis clínicos rigurosos y bien controlados. De ahí que los estudios mostrados en esta revisión reflejan la antigüedad del esfuerzo científico en recolección de datos, las diversas presentaciones de cannabis disponibles para estudio, las diferentes vías de administración posibles, sin híbridos o dosis estandarizadas, con aclaratoria de resultados dirigidos a generar recomendaciones, ya que no reproducen resultados entre sí.
La rama de la oncología sigue siendo predominante en el uso de soporte con cannabis medicinal, como muestran las múltiples directrices internacionales vigentes. Esto ha permitido la aceptación legislativa con sus respectivos lineamientos según cada país, destacando el uso previo diagnóstico por un médico capacitado en uso de cannabis medicinal, que emita una indicación basada en la evidencia actual, así como la identificación de productos adecuadamente etiquetados en cuanto a su empresa productora, formulación química, certificación de materia prima libre de pesticidas o metales pesados, concentración de canabinoides, vía de uso, fecha de caducidad y advertencia a menores de edad. Este especialista de la salud debe estar en la capacidad de explicar tanto los beneficios como limitaciones del producto, nunca siendo sustitutivo de los tratamientos oncológicos estandarizados, sin causar interferencia a la farmacocinética o intervención terapéutica y los resultados esperados de los mismos.
En el aspecto legal, el soporte de investigaciones desde finales de los años 1970 sobre el uso del cannabis medicinal, en el área oncológica, ha permitido su crecimiento exponencial en los últimos 5 años, a pesar de los países cuyas legislaciones sobre drogas se apegan a la vigente desde 1961, clasificada como como droga de potencial abuso y dependencia, sin beneficio médico. En respuesta a esto, en abril de 2024 se inicia la propuesta de replanteamiento de la posición del cannabis ante la Administración de Control de Drogas de Estados Unidos (DEA) para una reclasificación a droga tipo III, que le otorgaría un potencial de abuso menor, reconociendo el uso médico, con consecuente viabilidad de acceso a investigaciones con una mayor población, lo cual posibilita estudios multicéntricos, comparativos y de resultados reproducibles que proporcionen respuestas sólidas a las interrogantes actuales.
Por su parte, el gremio médico debe informarse de esta herramienta de soporte, de antigüedad milenaria, para demandar mayor desarrollo de la investigación sobre su farmacocinética, beneficios y perfil de efectos secundarios del cannabis medicinal, así como evidencia de su interacción con los diferentes protocolos oncológicos quirúrgicos, médicos, radioterapia e inmunoterapia establecidos.
El uso del cannabis medicinal debe mantenerse sin estigmatización del usuario que lo solicita, quien, por el contrario, busca un alivio no encontrado en tratamientos convencionales. Además, se debe reconocer que el paciente oncológico en nuestro tiempo tiene mayor sobrevida, y se transforma en una enfermedad crónica, por lo que debe coexistir con secuelas o efectos secundarios a largo plazo de los tratamientos recibidos o de mantenimiento; ante esto, el cannabis es una mejoría a síntomas físicos, neuropsiquiátricos, como náuseas, vómitos, anorexia, dolor crónico, ansiedad e insomnio, ya sea usado de forma aislada o en conjunto con medicación convencional.
Referencias
- Centro Nacional de Salud Complementaria e Integrativa. Disponible en la web: https://www.nccih.nih.gov/about
- Claudia M. Witt, Lynda G. Balneaves. A Comprehensive Definition for Integrative Oncology. Disponible en la web: https://academic.oup.com/jncimono/article/2017/52/lgx012/4617827
- Sociedad de Oncología Integrativa, directrices. Disponible en la web: https://integrativeonc.org/practice-guidelines/
- Éliana Lapierre, Adrian S Monthony. Genomics-based taxonomy to clarify cannabis classification. Disponible en la web: https://cdnsciencepub.com/doi/full/10.1139/gen-2023-0005?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
- Catalina Christensen, Martin Rose. Decoding the Postulated Entourage Effect of Medicinal Cannabis: What It Is and What It Isn’t. Disponible en la web: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10452568/
- Danielle Brown, Michael Watson. Pharmacological evidence of medicinal cannabis in oncology: a systematic review. Disponible en la web: Supportive Care in Cancer https://doi.org/10.1007/s00520-019-04774-5.
- Convención Única de Estupefacientes de 1961. Organización de Naciones Unidas. Disponible en la web: https://www.incb.org/documents/Narcotic-Drugs/1961-Convention/convention_1961_es.pdf.
- W A Devane, F A Dysarz 3rd. Determination and characterization of a cannabinoid receptor in rat brain. Disponible en la web: https://molpharm.aspetjournals.org/content/34/5/605.long.
- Munro, S., Thomas, K. & Abu-Shaar, M. Molecular characterization of a peripheral receptor for cannabinoids. Disponible en la web: Nature. https://doi.org/10.1038/365061a0
- Administración de Alimentos y Medicamentos de los Estados Unidos (FDA). Base de datos. Disponible en la web: https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/018651s029lbl.pdf
- Devane WA, Haight A. Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science. 1992. Disponible en la web: https://www.science.org/doi/10.1126/science.1470919?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed.
- Pertwee RG. Pharmacology of cannabinoid CB1 and CB2 receptors. Pharmacol Ther. 1997;74(2):129-80. Disponible en la web: doi: 10.1016/s0163-7258(97)82001-3. PMID: 9336020.
- Food and Drugs Administration, Epidiolex 2018. Disponible en la web: https://www.accessdata.fda.gov/drugsatfda_docs/label/2018/210365lbl.pdf
- Ley Orgánica Reformatoria al Código Orgánico Integral Penal (T224127). Disponible en la web: https://www.asambleanacional.gob.ec/es/multimedios-legislativos/40176-ley-organica-reformatoria-al-codigo.
- Resolución ARCSA-DE-002-2021-MAFG “Normativa Técnica Sanitaria para la regulación y control de productos terminados de uso y consumo humano que contengan Cannabis No Psicoactivo o Cáñamo, o Derivados de Cannabis No Psicoactivo o Cáñamo”. Disponible en la web: https://www.controlsanitario.gob.ec/wp-content/uploads/downloads/2021/02/Resolucion-ARCSA-DE-002-2021-MAFG_Normativa-Tecnica-Sanitaria-para-la-regulacion-y-control-de-productos-terminados-de-uso-y-consumo-humano-que-contengan-Cannabis-No-Psicoactivo-o-Canamo.pdf
- Chang AE. Delata-9-tetrahydrocannabinol as an antiemetic in cancer patients receiving high-dose methotrexate. A prospective, randomized evaluation. Ann Intern Med. 1979 Dec;91(6):819-24. doi: 10.7326/0003-4819-91-6-819. PMID: 293141.
- Engels FK. Medicinal cannabis does not influence the clinical pharmacokinetics of irinotecan and docetaxel. Oncologist. 2007 Mar;12(3):291-300. doi: 10.1634/theoncologist.12-3-291. PMID: 17405893.
- Abrams DI. Cannabinoid-opioid interaction in chronic pain. Clin Pharmacol Ther. 2011 Dec;90(6):844-51. doi: 10.1038/clpt.2011.188. Epub 2011 Nov 2. PMID: 22048225.
- Zhang, Han & Xie. (2018). Association of Marijuana Use With Psychosocial and Quality of Life Outcomes Among Patients With Head and Neck Cancer. JAMA Otolaryngology – Head and Neck Surgery. 144. 10.1001/jamaoto.2018.0486.
- Cannabis-In-Cachexia-Study-Group; Strasser F. Comparison of orally administered cannabis extract and delta-9-tetrahydrocannabinol in treating patients with cancer-related anorexia-cachexia syndrome: a multicenter, phase III, randomized, double-blind, placebo-controlled clinical trial from the Cannabis-In-Cachexia-Study-Group. J Clin Oncol. 2006 Jul 20;24(21):3394-400. doi: 10.1200/JCO.2005.05.1847. PMID: 16849753.
- Johnson JR. Multicenter, double-blind, randomized, placebo-controlled, parallel-group study of the efficacy, safety, and tolerability of THC:CBD extract and THC extract in patients with intractable cancer-related pain. J Pain Symptom Manage. 2010 Feb;39(2):167-79. doi: 10.1016/j.jpainsymman.2009.06.008. Epub 2009 Nov 5. PMID: 19896326.
- Brisbois TD. Delta-9-tetrahydrocannabinol may palliate altered chemosensory perception in cancer patients: results of a randomized, double-blind, placebo-controlled pilot trial. Ann Oncol. 2011 Sep;22(9):2086-2093. doi: 10.1093/annonc/mdq727. Epub 2011 Feb 22. PMID: 21343383.
- Portenoy RK. Nabiximols for opioid-treated cancer patients with poorly-controlled chronic pain: a randomized, placebo-controlled, graded-dose trial. J Pain. 2012 May;13(5):438-49. doi: 10.1016/j.jpain.2012.01.003. Epub 2012 Apr 5. PMID: 22483680.
- Directrices cannabis medicinal para tratamientos de los síntomas en cuidados paliativos, Australia, 2017. Disponible en la web: https://www.tga.gov.au/sites/default/files/guidance-use-medicinal-cannabis-treatment-palliative-care-patients-australia.pdf
- Alderman B. Multinational Association of Supportive Care in Cancer (MASCC) expert opinion/consensus guidance on the use of cannabinoids for gastrointestinal symptoms in patients with cancer. Support Care Cancer. 2022 Dec 16;31(1):39. doi: 10.1007/s00520-022-07480-x. PMID: 36525085.
- To J. MASCC guideline: cannabis for cancer-related pain and risk of harms and adverse events. Support Care Cancer. 2023 Mar 6;31(4):202. doi: 10.1007/s00520-023-07662-1. Erratum in: Support Care Cancer. 2023 May 6;31(6):323. doi: 10.1007/s00520-023-07789-1. PMID: 36872397.
- De Feo G. Multinational Association of Supportive Care in Cancer (MASCC) guidelines: cannabis for psychological symptoms including insomnia, anxiety, and depression. Support Care Cancer. 2023 Feb 21;31(3):176. doi: 10.1007/s00520-023-07628-3. PMID: 36809575.
- Bell AD. Clinical Practice Guidelines for Cannabis and Cannabinoid-Based Medicines in the Management of Chronic Pain and Co-Occurring Conditions. Cannabis Cannabinoid Res. 2024 Apr;9(2):669-687. doi: 10.1089/can.2021.0156. Epub 2023 Mar 27. PMID: 36971587; PMCID: PMC10998028.
- Braun IM. Cannabis and Cannabinoids in Adults With Cancer: ASCO Guideline. J Clin Oncol. 2024 May 1;42(13):1575-1593. doi: 10.1200/JCO.23.02596. Epub 2024 Mar 13. PMID: 38478773.
Cómo citar el presente artículo:
Polanco Y. Cannabis medicinal como parte de la oncología integrativa. Revisión Bibliográfica. Indexia. Diciembre 2024.
Todos los artículos se publican bajo la licencia Creative Commons Atribución 4.0 Internacional (CC-BY 4.0), lo que permite compartir y adaptar el contenido siempre que se dé el crédito adecuado a los autores y a la revista.
